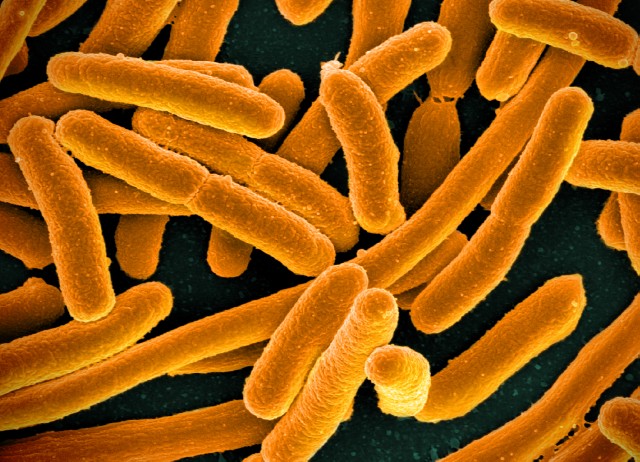
Què són els bacteris?
Les malalties infeccioses que patim els humans son causades per microorganismes patògens com els bacteris, els virus, els paràsits o els fongs. Aquestes malalties es poden transmetre, directament o indirectament, d’una persona a una altra.
Avui us parlarem dels bacteris. Els bacteris són microorganismes unicel·lulars, no visibles a simple vista i no posseeixen nucli, es reprodueixen per divisió cel·lular i poden presentar diferents formes com ara un bastó (bacils), rodons(cocs), amb forma de llevataps o tirabuixó (vibrions), o bé amb forma d’hèlix o espiral (espirils).

Dels bacteris n’hi ha que no generen cap malaltia i es troben com a habitants normals en tots els éssers vius (de fet s’estima que el nostre cos conté uns 40 bilions de bacteris que equivalen a 1 o 2 kilograms de pes i son necessaris pel bon funcionament dels nostres òrgans) i d’altres que son patògens, és a dir, que causen algun tipus de malaltia.
Tot i que no totes són mortals, hi ha alguns bacteris perillosos que poden ser molt perjudicials per a l’organisme i provocar diferents danys si no es detecten i tracten a temps.
Quins són els bacteris més perillosos i mortals?
Els principals bacteris perillosos i mortals:
- Acinetobacter baumannii, provoca milers de morts l’any
- Pseudomonas aeruginosa, provoca infeccions pulmonars severes o septicemia.
- Campylobacter, que causa la campilobacteriosi
- Salmonella, que causa la salmonel·losi
- Escherichia coli, enteropatogen
- Helicobacter pylori, habita a l’estomac i pot causar: Úlcera sèptica, irritació de còlon…
En un estudi publicat per la revista ‘The Lancet’ (1) es calcula que els bacteris resistents a medicaments van suposar 1,27 milions de morts directes i van tenir algun paper en almenys 4,95 milions de morts el 2019, fet que suposa un nombre més gran de morts respecte a les que s’associen a altres malalties com la sida o la malària. La investigació reflecteix que la sida i la malària van causar 860.000 i 640.000 morts respectivament durant l’any objecte de l’estudi.
La previsió de morts l’any 2050 com a causa de bacteris resistents, s’estima que serà d’uns 10 milions de persones a tot el món.
Com podem combatre’ls?
Quan tenim una infecció deguda a un bacteri, prenem antibiòtics, que son fàrmacs (molècules) capaços d’aturar la divisió cel·lular i per tant de que s’estengui la infecció i/o d’acabar amb el propi bacteri.
Actualment els antibiòtics que fem servir son d’ampli espectre, que vol dir que son capaços de “matar” diferents tipus de bacteris, i quan un no funciona ens en recepten un altre, també d’ampli aspecte, que normalment es capaç de “matar” una varietat diferent de bacteris.
Aquests bacteris, evolucionen i es fan més resistents als antibiòtics actuals, és per això que els metges ens recomanen no prendre antibiòtics a la primera de canvi.
L’OMS estima que al 2050 la resistència als antibiòtics serà la principal causa de mort.
Trobar antibiòtics nous no és fàcil ja que el mecanisme molecular d’acció dels darrers antibacterians d’ampli espectre té 40 anys d’antiguitat, malgrat els enormes esforços realitzats en farmàcia per trobar-ne de nous.
Caps de serveis sanitaris nacionals, organitzacions professionals de malalties infeccioses i experts en malalties infeccioses adverteixen que estem davant d’un retorn a una era pre-antibiòtica i les infeccions per bacteris (superbugs) augmenten tant en gravetat com en freqüència, i ara calen nous medicaments per tractar-los.
Els antibiòtics específics per bacteris patògens concrets representen un enfocament innovador per desenvolupar fàrmacs antiinfecciosos i tenen el potencial de donar lloc a una generació totalment nova d’antibiòtics.
Hi ha diverses tècniques per a la creació de nous fàrmacs, una d’elles és mitjançant la creació de noves molècules (aquesta feina la fan els bioquímics), també es poden patentar nous usos específics de molècules ja conegudes, per exemple l’Aspirina (L’àcid acetilsalicílic) ara sabem que també es pot usar com Anticoagulant i una altra tècnica que és més laboriosa és la tècnica de l’Screening, que us expliquem tot seguit.
Que és un Screening o cribatge?
De la mateixa manera que antigament les trementinaires del Pirineu anaven de poble en poble amb la seva col·lecció d’herbes per tractar tot tipus de malalties, avui en dia hi ha empreses que disposen de col·leccions de milers de compostos naturals dels quals encara no sé n’ha trobat cap ús terapèutic.
Així doncs, per una banda tenim els bacteris patògens (que causen malalties) i per l’altra col·leccions de compostos naturals.
L’screening consisteix en provar cadascun dels bacteris que volem combatre contra cadascun dels compostos naturals de la col·lecció per veure quin efecte té.
Sí una col·lecció, per exemple, te 200.000 compostos i l’estudi comprèn 20 bacteris, estem parlant que s’han de realitzar de 4 milions de proves amb maquinària i personal molt especialitzat.
Les dades obtingudes, són voluminoses i també s’han de tractar de manera automatitzada per tal d’obtenir els millors candidats per passar a la següent fase del cribratge.
Quines característiques ha de tenir un bon compost?
En les següents fases, buscarem compostos que a l’igual que un triatleta ha de saber nedar, córrer i anar en bicicleta, voldrem compostos que siguin bons i de manera equilibrada en tres aspectes:
- No permetin el creixement o matin el bacteri o bacteris objectiu amb la menor dosi possible
- Que no siguin tòxics per a teixits d’òrgans vitals
- Que siguin ben tolerats per un petit primer ésser viu
I ara què? Quins son els següents passos?
A partir d’aquí, tot compost que s’hagi descobert encara té un llarg camí per recórrer, que pot durar molts anys fins que arribi a les nostres farmàcies.
Abans de començar a assajar amb humans, primerament el medicament ha de passar una sèrie de fases prèvies de seguretat i tolerància en animals.
Un cop superades, han de passar les 3 fases d’un assaig clínic que son estudis de nous medicaments per poder saber la seva tolerància i eficàcia , però això ja són figues d’un altre paner.
Per a més informació sobre els Assaigs clínics farmacològics podeu llegir aquest article (https://santpaumemoryunit.com/ca/assaigs-clinics/)
Com podeu deduir, la descoberta d’un nou fàrmac és un procés molt llarg i laborios, que passa per moltíssimes fases per tal de garantir al màxim que no sigui pitjor el remei que l’enfermetat i que cal ser conscients que no sempre acaba amb èxit.
L’inLab FIB, de la Universitat Politècnica De Catalunya · Barcelona Tech – UPC, col.labora amb la companyia ABAC Therapeutics des de l’any 2020 en el desenvolupament d’una plataforma pròpia de descobriment de fàrmacs per a identificar antibiòtics nous orientats a combatre els bacteris multi-resistents anomenada PasNas.
Bibliografia
- (1) The Lancet: Global burden of bacterial antimicrobial resistance in 2019: a systematic analysis https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(21)02724-0/fulltext
- https://www.flsida.org/ca/malalties-infeccioses
- https://acsa.gencat.cat/ca/detall/article/Bacteris-00004
- https://santpaumemoryunit.com/ca/assaigs-clinics/
- https://mejorconsalud.as.com/las-9-bacterias-peligrosas-mas-daninas-humano/
- https://www.eldiario.es/sociedad/muertes-anuales-bacterias-resistentes-medicamentos-superan-causadas-sida-malaria_1_8670535.html
- https://inlab.fib.upc.edu/ca/plataforma-de-descobriment-de-farmacs-pasnas